研究背景:
心肌梗死(MI)是全世界心血管疾病发病和死亡的主要原因。MI导致心肌细胞大量损伤,最终破坏了心肌组织的结构和功能,导致心脏功能障碍。传统治疗无法有效逆转梗死后心肌组织的损伤和功能障碍。基于水凝胶贴片(ECP)已被证明可以有效地构建修复性微环境,从而在梗死心肌上桥接电和机械刺激,可以防止心肌变薄和扩张,改善心脏功能。通过考虑和优化生物相容性、机械性能和导电性等因素,ECP可以成功促进心肌修复。
基于此,南方医科大学邱小忠教授/王乐禹教授团队在《ADVANCED FUNCTIONAL MATERIALS》期刊发表题目为“A Strongly Robust Chitosan-Based Programmed Control Functional Hydrogel Improved Mitochondrial Function and Pro-Vascularization for Adaptive Repair of Myocardial Infarction”的研究文章。

本研究构建了一种基于壳聚糖(CS)程序控制功能化的ECP(CS/TA@PAs-Eu),用于修复MI。CS作为一种生物相容性良好的多糖,具有良好的降解性,并且其含有的游离氨基可以引发阴离子交换,形成离子传导网络。通过将CS水凝胶中的氢键结构设计为可控制的,来构建稳定的机械性能,并满足ECP的稳健性要求。此外,通过引入具有抗氧化和促血管生成作用的天然小分子,如α-硫辛酸(TA)、原花青素(PA)以及功能性金属离子Eu3+,可以进一步改善ECP的生物活性和修复效果。该ECP利用冰模板辅助构建CS水凝胶,并通过嵌入聚(TA)网络、PAs的交联作用以及PAs与Eu3+的螯合作用来增强其离子电导率、改善线粒体功能,并具有抗氧化和促血管生成特性,最终评价其对梗死心肌的治疗效果及心功能的恢复情况。
研究方法:
文中采用64通道电标测技术(Electrical Mapping,MappingLab Limited,UK)评估大鼠心脏左心室正常和梗死心肌边界区域的传导时间、速度、场电位振幅等电信号的变化。
研究结果:
1、CS/TA@PAs-Eu 水凝胶的制备和表征
首先,通过调控酸性到碱性环境的转变,实现了壳聚糖水凝胶的有序构建,从而获得了具有良好机械性能和柔韧性的水凝胶网络。在低温环境下,由于氢氧根离子的程序化渗透,通过冰晶模板的强聚合氢键形成了坚固的水凝胶网络(见方案1)。采用这种程序化氢键构建的水凝胶表现出强大的机械稳健性,有望为梗死心肌提供持久的机械支撑。同时,利用辅酶Q10的热开环效应构建了聚(TA)网络,并引入PAs分子来构建CS/TA@PAs-Eu水凝胶的双网络结构(见方案2)。
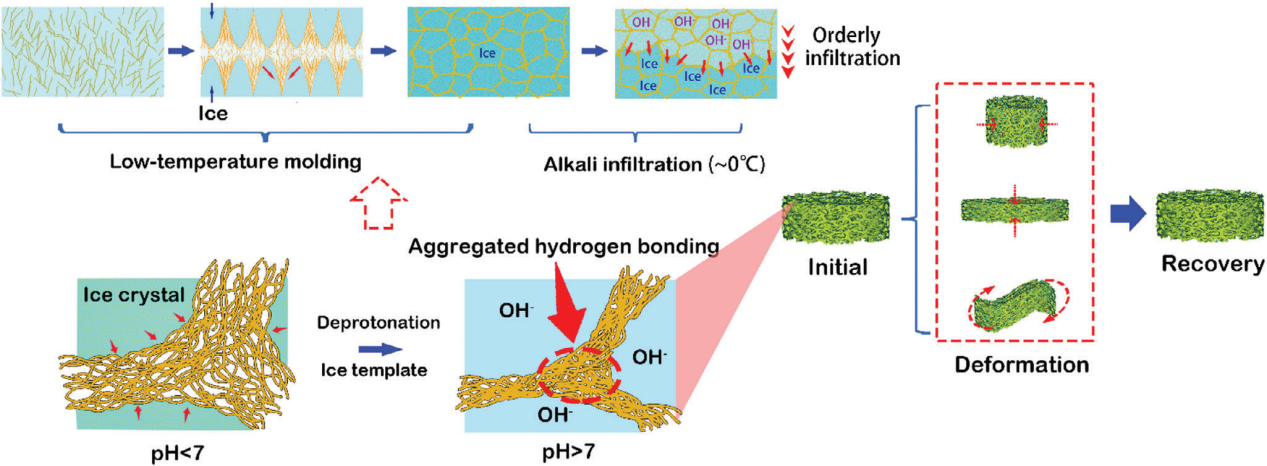
方案1. 低温碱性渗透诱导的程序化氢键构建CS水凝胶
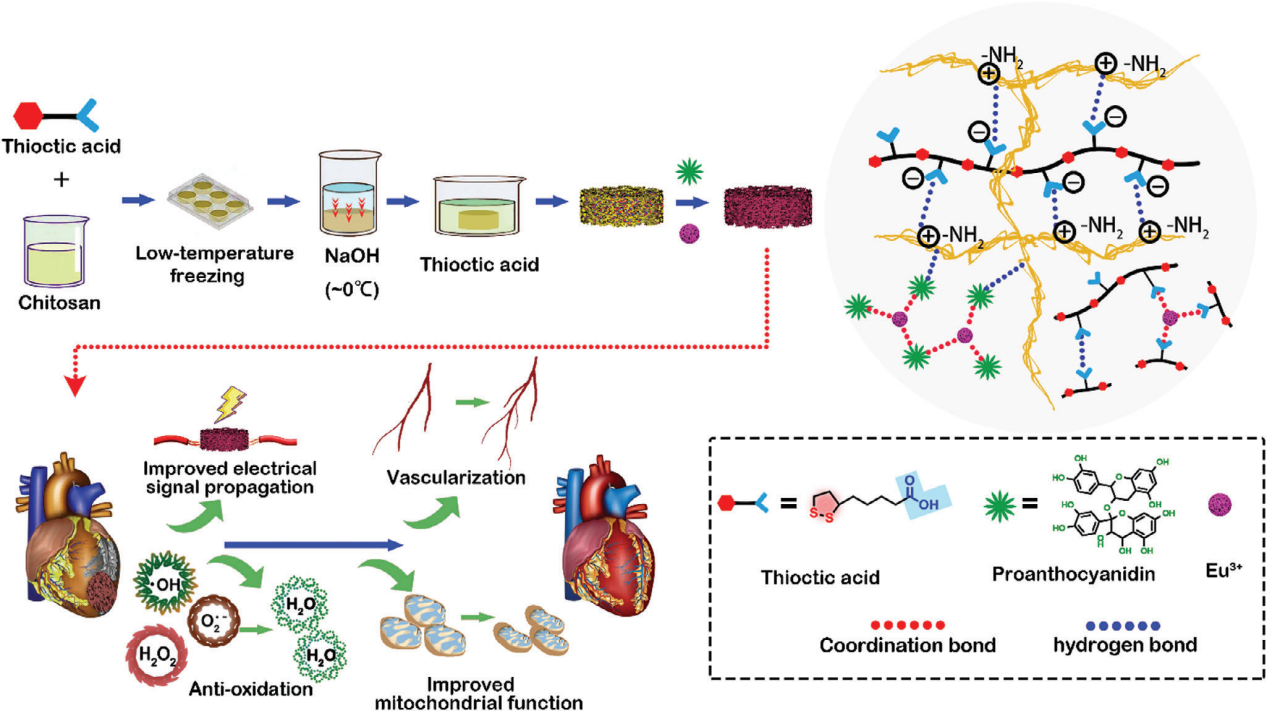
方案2. 关于功能化CS水凝胶(CS/TA@PAs-Eu)构建及其在心肌梗死修复中的应用的示意图说明
通过冰晶模板的辅助构建,水凝胶具有相互连接的大孔结构。PAs的添加进一步交联了CS分子,导致孔结构的缩小。TA的嵌入使得水凝胶呈现黄色,而PAs的均匀锚定则使水凝胶由黄色过渡为红色。进一步的实验结果表明,CS/TA@PAs-Eu水凝胶具有良好的机械抗性和稳健性,其通过程序化氢键构建的网络使得水凝胶具有稳定的结构。此外,水凝胶的大孔结构有助于细胞的附着,并且对应变具有良好的恢复能力。通过添加PAs和Eu3+,水凝胶的电导性得到提高,为其在心肌组织中的应用提供了基础。这些结果证实,通过程序化氢键构建的CS/TA@PAs-Eu水凝胶具有稳定的凝胶结构(图1)。

图1. 水凝胶的数字照片和扫描电子显微镜图像
2、体外CMs的成熟和功能化
接下来,评估水凝胶对心肌细胞(CMs)存活和成熟度的影响。结果表明,基于壳聚糖的水凝胶具有良好的细胞相容性,能维持CMs的高存活率。添加了TA、PAs和Eu3+等功能组分后,水凝胶对CMs的存活和成熟度有进一步促进作用。此外,水凝胶的功能组分释放效应对CMs的生长环境起到持续影响,进一步促进了细胞的成熟和功能化。在细胞水平上,水凝胶对CMs的α-肌动蛋白和CX43蛋白表达具有积极影响,有助于细胞间的连接和电耦合,从而提高了细胞的自发收缩能力。这些结果证明了功能化水凝胶在促进CMs存活和成熟方面的生物学效应,为MI修复提供了新的治疗策略。

图2. 水凝胶上CMs的Live/Dead染色,并根据Live/Dead染色图像定量测定细胞活力
3、水凝胶的抗氧化性能、线粒体保护功能及促血管化
随后又评估了水凝胶的抗氧化能力,发现CS/TA@PAs-Eu水凝胶对多种自由基具有良好的清除效果,包括H2O2、·OH、·O2−和DPPH。壳聚糖本身具有一定的抗氧化活性,而添加了TA和PAs后,水凝胶的抗氧化性能得到了进一步增强。实验结果还显示,CS/TA@PAs-Eu水凝胶能够有效清除细胞内ROS,改善线粒体功能,并提高细胞的ATP水平。这些发现表明,CS/TA@PAs-Eu水凝胶用于清除MI微环境中的过量ROS,并改善线粒体功能具有潜力。
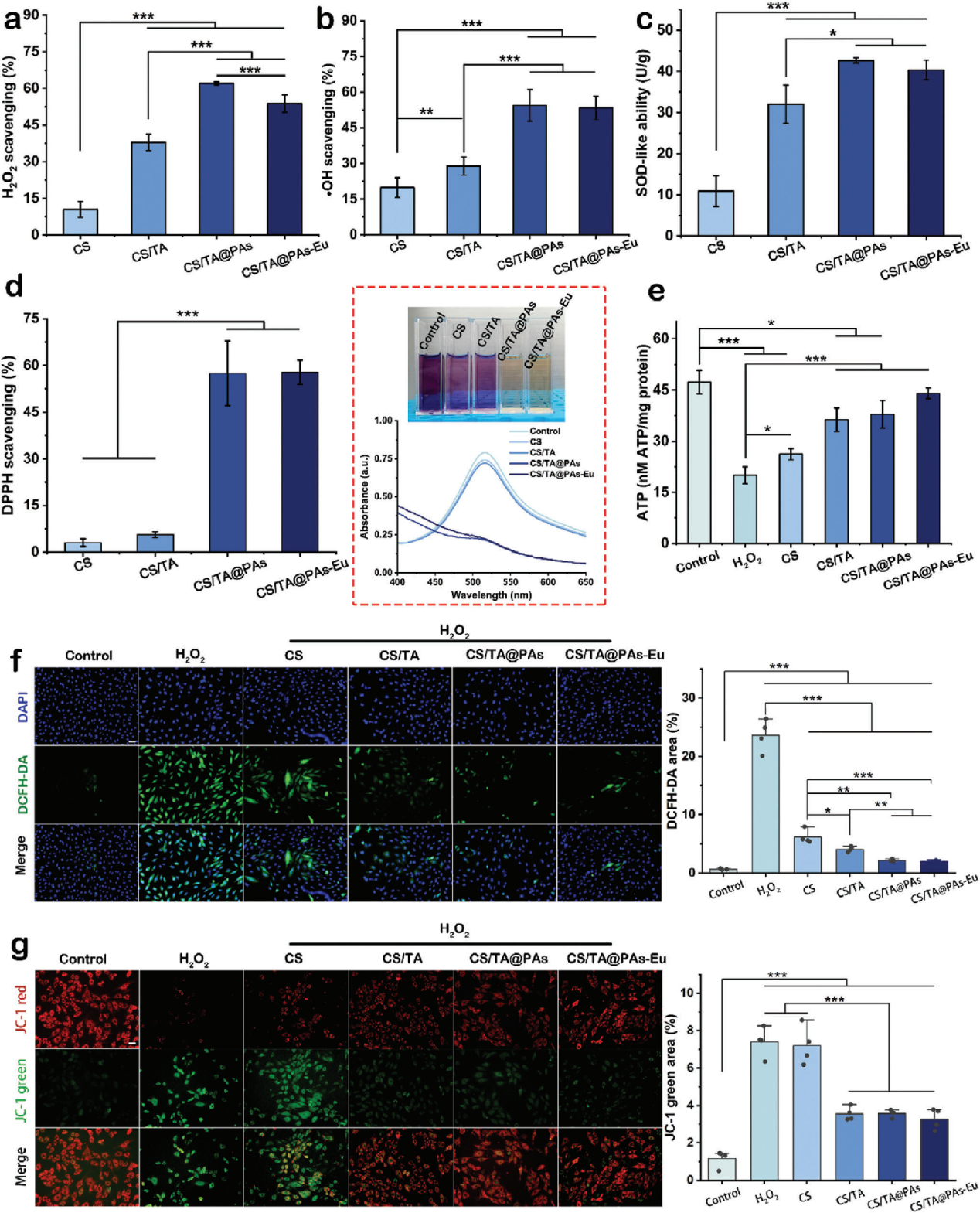
紧接着评估水凝胶对人脐静脉内皮细胞(HUVEC)的影响,特别是其对血管再生的作用。结果显示,CS/TA@PAs-Eu水凝胶具有良好的生物相容性,能促进HUVEC管道形成并增强细胞迁移能力。此外,添加Eu3+可以改善水凝胶对HUVEC的存活率,同时促进血管生成。总体而言,这些发现表明所构建的功能性水凝胶具有改善梗死心肌血管再生的潜力。

图4. 水凝胶处理下HUVECs的Live/Dead染色和细胞增殖活性
4、水凝胶对梗死后心功能的改善
接下来评估水凝胶对心肌梗死后心脏功能的恢复效果。实验结果表明,水凝胶处理能改善大鼠的存活率,并显著增强心脏的收缩活动和壁厚。特别是CS/TA@PAs-Eu水凝胶处理组表现出最显著的修复效果。此外,水凝胶还抑制了心肌组织的纤维化,并保持了心室壁厚度。这些结果表明,CS/TA@PAs-Eu水凝胶有望通过促进心脏泵血能力、抑制心室重塑以及对梗死心肌的修复,改善心力衰竭(图5)。

图5. 水凝胶植入前后的心脏的超声心动图图像
CS/TA@PAs-Eu水凝胶在心肌梗死(MI)修复过程中的改善效果可以归因于其多方面的干预作用。MI后早期的炎症反应是病理性ROS诱导的,主要源自受损的线粒体。因此,评估不同水凝胶处理组梗死心肌中线粒体形态的变化,结果显示,CS/TA、CS/TA@PAs和CS/TA@PAs-Eu水凝胶能更好地保护线粒体的完整性,减轻ROS对线粒体结构的损伤,并防止心肌细胞凋亡和损伤。此外,水凝胶处理显著降低了梗死心肌中ROS水平,并促进了电-收缩耦合的恢复,维持了心肌电生理功能(图6)。对梗死心脏中电信号传导的测量结果显示,CS/TA@PAs-Eu水凝胶对电信号传导的改善效果最为显著(图S15)。水凝胶处理还促进了梗死心肌的血管生成,并通过调节巨噬细胞极化来抑制纤维化。总的来说,CS/TA@PAs-Eu水凝胶的功能成分持续释放有助于改善MI修复的多个方面,包括线粒体功能、抗氧化和促血管生成。此外,水凝胶在主要组织(肝脏、脾脏、肺和肾脏)中的生物安全性在植入后4周进行了评估,结果显示每组主要器官的组织切片没有显著差异。这些结果表明水凝胶在体内具有良好的生物相容性。

图6. MI三维线粒体结构的透射电镜图像
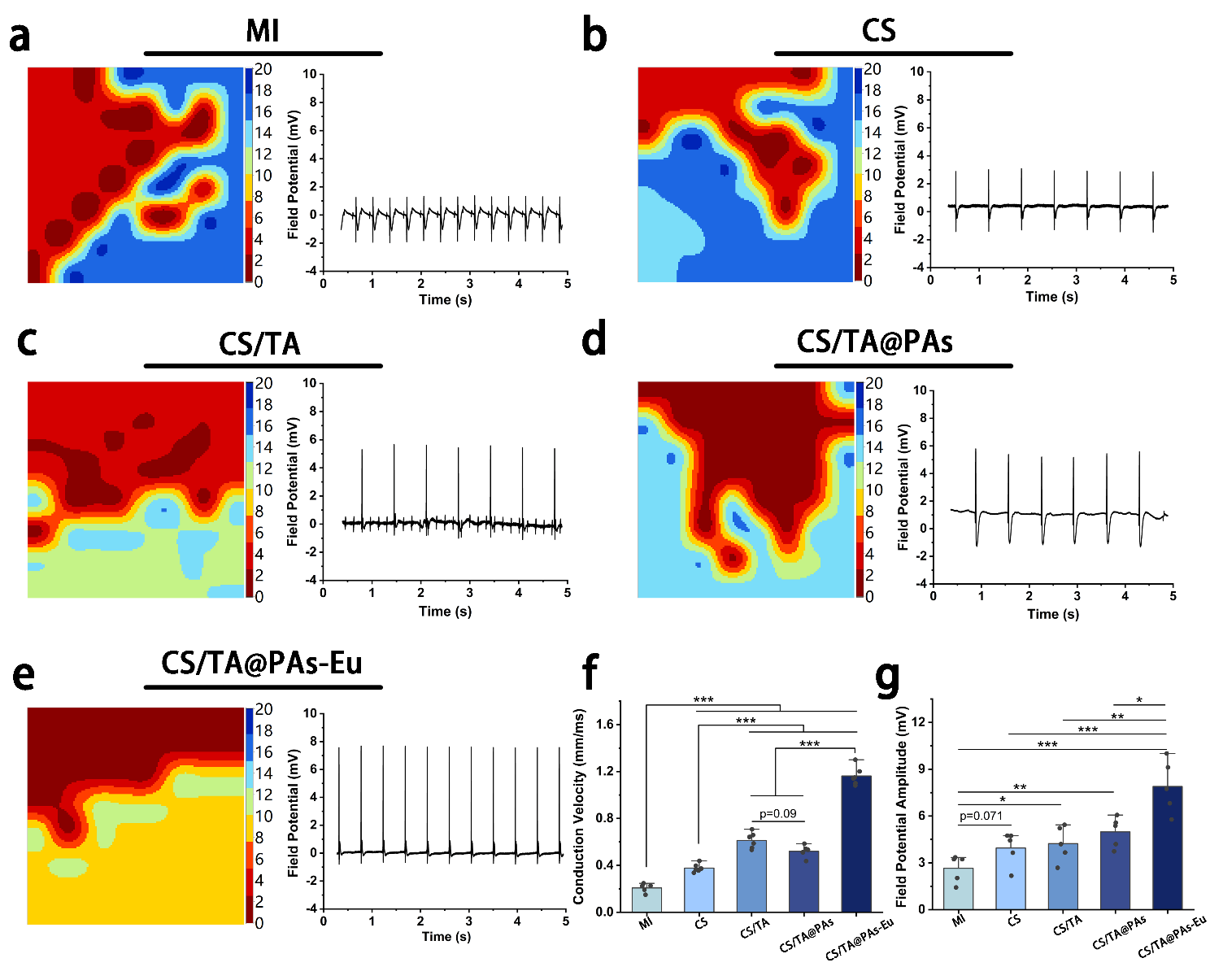
图S15. 使用64通道电标测系统检测梗死4周时不同组Langendorff灌注心脏的电标测图像,以及梗死部位记录的局部场电位电图
综上,CS/TA@PAs-Eu水凝胶可有效改善心肌梗死的修复。通过一系列实验结果表明,CS/TA@PAs-Eu水凝胶具有较强的机械性能和生物相容性,有助于心肌细胞的成熟和功能化。在动物实验中,该水凝胶表现出对心肌梗死的适应性修复作用,包括改善线粒体功能、抗氧化、电生理重建和促进血管生成等方面。总的来说,这项研究为MI的治疗提供了一个新的潜在方案。