背景:
心肌梗死(MI)仍是全球死亡的主要原因之一。冠脉阻塞会产生缺血-缺氧反应,导致心肌细胞损伤及细胞因子、趋化因子和生长因子上调。重要的是,基质细胞衍生因子-1α(SDF-1α),也称为趋化因子CXCL12,已被证明通过结合趋化因子受体4型(CXCR4)来募集骨髓来源的干细胞进行心脏修复。SDF-1α/CXCR4 轴通过将内源性干细胞募集到缺血组织中,有助于心肌梗死 (MI) 后的心肌保护。然而,炎症巨噬细胞也会同时募集,加重心肌损伤。更严重的是,炎症的增加导致心肌细胞电耦联异常,如心室传导不均匀和传导速度减慢。因此募集干细胞但阻断炎症是重要的。
近日,南方医科大学第十附属医院(东莞市人民医院)李振华研究员联合美国哥伦比亚大学程柯教授团队,在《Advanced Materials》发表了题目为Pericardial Delivery of SDF-1α Puerarin Hydrogel Promotes Heart Repair and Electrical Coupling 的相关研究论文。
在这项研究中,SDF-1α包裹葛根素(PUE)水凝胶(SDF-1α@PUE)能够增强内源性干细胞归巢,同时将募集的单核细胞/巨噬细胞极化为修复表型 M2 型,调节细胞间耦联并改善电传导。利用改良的“土壤”募集的干细胞,通过防止恶化、促进新生血管结构和减少梗死面积来改善心脏功能。这些发现证明了一种很有前途的心肌梗死治疗平台,不仅可以促进心脏再生,还可以降低心律失常的风险。
方法:
文中采用荧光标测和电标测技术联合(Optical Mapping&Electrical Mapping, MappingLab Limited, UK)检测不同大鼠模型的心脏电传导、动作电位以及钙瞬变信号的变化。
结果:
2.1 SDF-1α@PUE水凝胶的制备及生物相容性和巨噬细胞极化能力
这一研究通过使用加热/冷却处理自组装的葛根素(PUE)形成温度敏感水凝胶,成功实现了SDF-1α的高效递送。通过四种不同浓度的PUE水凝胶的比较,选择PUE-1.8%的凝胶进行后续应用,证明其在37°C下的稳定性和机械强度适用于心脏修复。通过电静电吸附效应将正电的SDF-1α和负电的PUE物理混合,形成了SDF-1α@PUE水凝胶,该凝胶在40°C下自组装成三维网络结构,有助于药物负载。在体外和体内研究中,SDF-1α@PUE水凝胶对SDF-1α的降解具有保护作用,持续释放时间可达一周,有望支持细胞向损伤部位的预期迁移。细胞活力和极化实验显示,SDF-1α@PUE水凝胶对心肌细胞和巨噬细胞都具有良好的生物相容性,并能促进M2型巨噬细胞的极化。进一步的体外模型实验证实SDF-1α@PUE水凝胶处理有助于血管形成和伤口愈合。通过体内成像和荧光图像,证明心内注射后SDF-1α@PUE水凝胶在梗死区迅速分散并长效释放,具有良好的生物分布和递送效果。

图1. SDF-1α@PUE水凝胶制剂及其体内生物分布
2.2 SDF-1α@PUE水凝胶对逆转炎症细胞募集引起的副作用的影响
在心肌梗死初期,急性炎症爆发,SDF-1α治疗可引导更多先天免疫细胞到梗死心肌。我们用SDF-1α@PUE水凝胶进行体内验证实验,结果显示其显著促进M2巨噬细胞活化,抑制M1巨噬细胞。多重验证包括流式细胞术、免疫荧光染色和Western Blotting,都一致表明PUE凝胶能有效抵消SDF-1α副作用,有助于抗炎和组织再生。ELISA结果显示,SDF-1α@PUE水凝胶显著降低IL-1β和IL-6,同时增加抗炎因子(IL-10和TGF-β)释放,证实其抗炎效力。
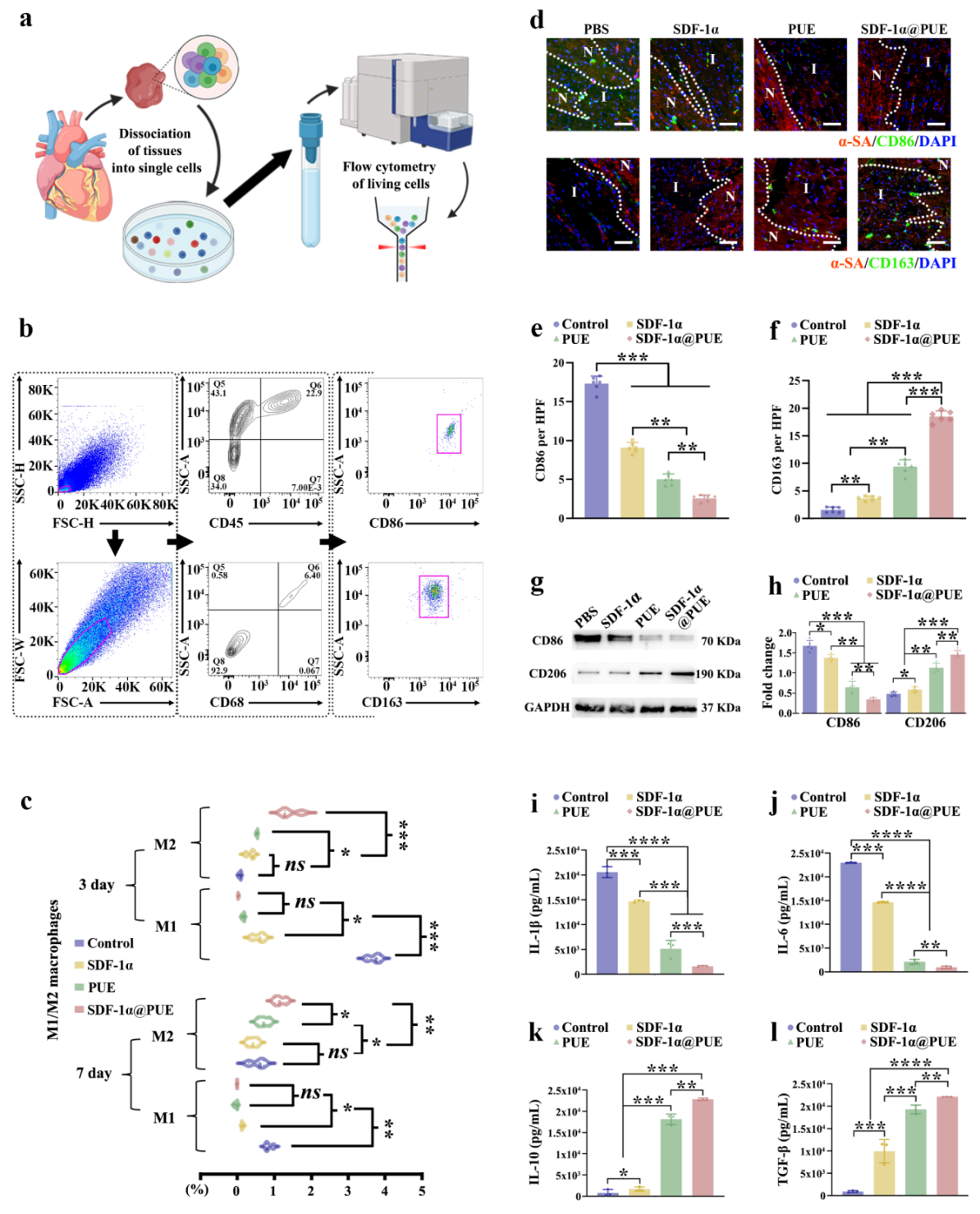
图2.SDF-1α@PUE水凝胶对逆转过度炎症的作用
2.3 SDF-1α@PUE介导的M1巨噬细胞发生极化是通过增加Cx43的表达来改善稳态
在心肌梗死后,SDF-1α@PUE水凝胶治疗成功地减轻了单核细胞前体分化的巨噬细胞对梗死区的损害,同时促进了心肌细胞的恢复。研究发现,该水凝胶能够显著提高缝隙连接蛋白43(Cx43)的表达,关键的心脏电信号传导分子,从而有助于维持心肌细胞的电活性。通过在巨噬细胞和心肌细胞共培养系统中研究M1/M2巨噬细胞对Cx43表达的影响,结果证实SDF-1α@PUE水凝胶的炎症调节作用对Cx43水平产生积极影响。此外,水凝胶治疗还通过减轻氧化应激、降低ROS水平来保护Cx43蛋白。

图3.SDF-1α@PUE调控心肌梗死后炎症和稳态对Cx43表达调控的影响
2.4 SDF-1α@PUE治疗后心律失常风险降低
研究表明,PUE水凝胶通过减缓SDF-1α/CXCR4轴加重的炎症,显著减少了心脏心律失常的风险。在荧光标测实验中,与梗死心脏组相比,SDF-1α@PUE水凝胶处理组APD90缩短,减少了心律失常的发生。此外,与梗死心脏组相比,SDF-1α@PUE水凝胶处理还加快了心脏电传导速度,改善了心脏电信号的传导。
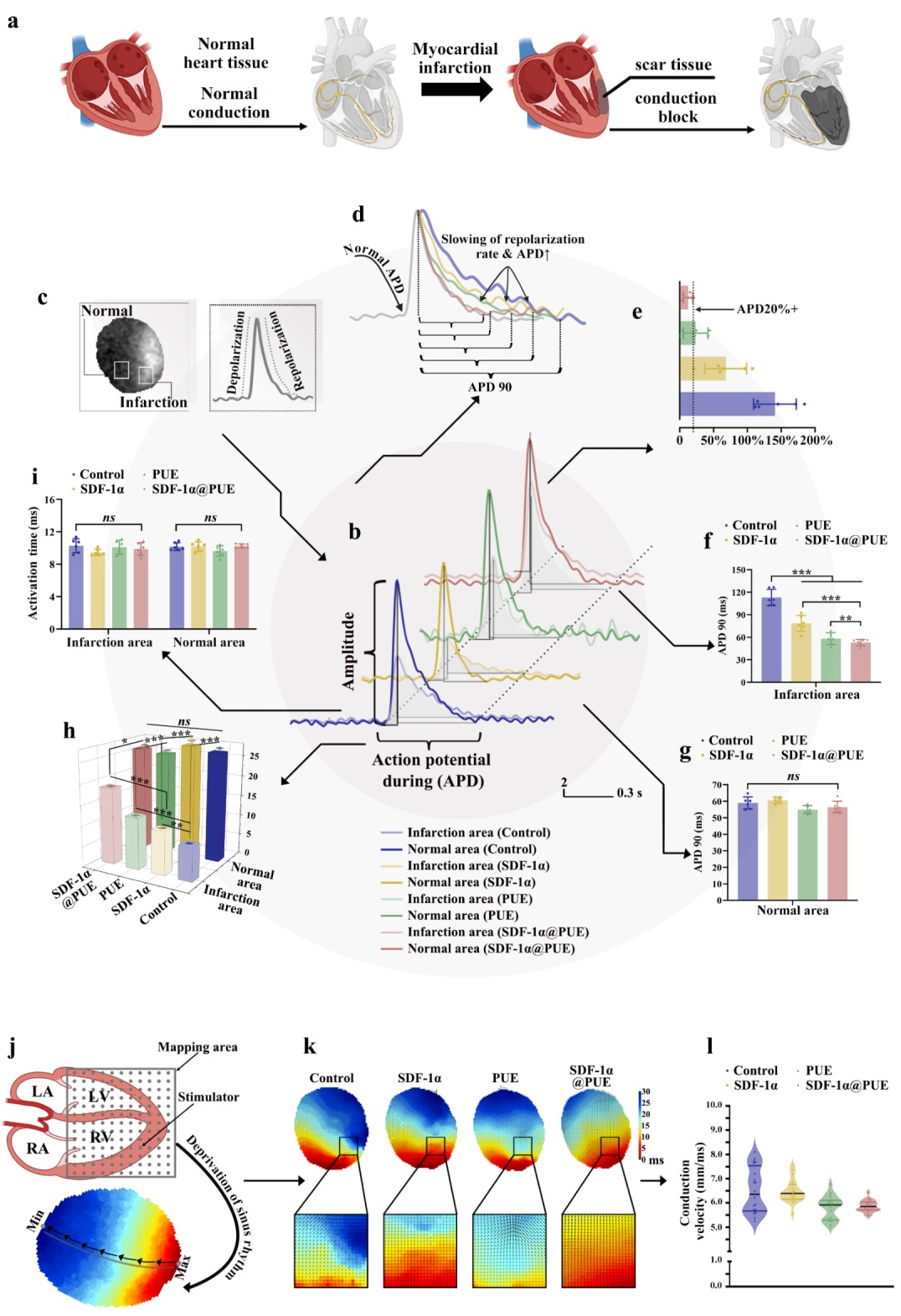
图4.SDF-1α@PUE治疗后心律失常风险降低
2.5 心脏兴奋-收缩耦合和电生理信号传导的调节
心肌细胞的收缩和舒张依赖于周期性的动作电位,而这一过程与钙相关。心肌功能受损部分归因于兴奋-收缩耦合(ECC)功能的改变,导致胞内Ca2+释放回收的时间和胞内Ca2+含量的变化。通过体外实验,研究了受损心肌细胞对炎症性ROS诱导的胞内钙浓度快速波动的机制。SDF-1α@PUE处理显著增强了Ca2+传导,减少了达到钙峰值所需的时间,并增加了钙脉冲的数量。光学标测实验证实了SDF-1α@PUE水凝胶处理组钙瞬变时程最短。电标测系统展示了SDF-1α@PUE组中梗死区域电传导正常,电信号从一个兴奋点到下一个有序的传递。心电图结果表明,SDF-1α@PUE组中的心脏节律稳定,与正常大鼠相似,而MI和SDF-1α处理组显示心脏缺血和异常心室去极化波形。

图5.心脏兴奋-收缩耦合和电生理信号的调节
2.6 SDF-1α的释放增加了血管生成
我们成功证实了PUE诱导梗死归巢巨噬细胞表型转换后,能够缓解心脏炎症微环境。研究发现,相较于其他对照组,SDF-1α@PUE处理组在Langendorff灌流的大鼠心脏中表现出更高的再灌注比率。PUE水凝胶的降解释放的SDF-1α,通过吸引内源干细胞,显著促进了新血管生成。流式细胞术分析结果显示,SDF-1α@PUE处理组有效协调体内髓系细胞的招募。该处理组中BM-MSCs和HSCs的比例显著增加,与SDF-1α单独处理组相比,这种效应在第7天更为显著。此外,通过Western Blotting和免疫荧光分析,我们发现SDF-1α@PUE水凝胶处理组促进了新血管生成相关标志物(CD31和α-SMA)的显著增加。
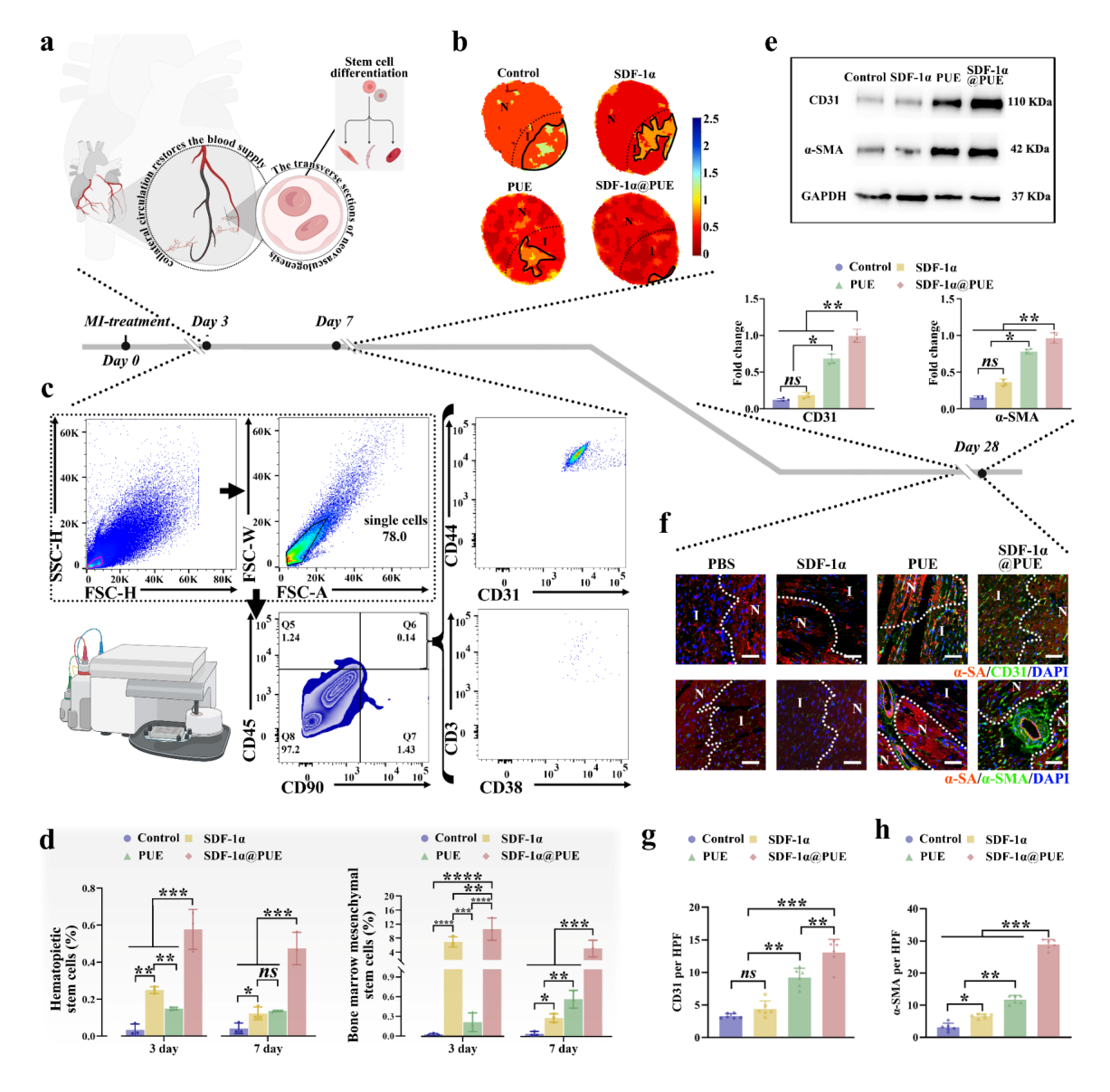
图6.SDF-1α的释放增加了血管生成
2.7 SDF-1α@PUE水凝胶对心肌梗死大鼠模型的疗效观察
通过在心肌梗死(MI)大鼠模型中进行iPC注射后展示SDF-1α@PUE水凝胶诱导的抗炎效应,观察到减少的促炎因子、增加的抗炎因子和Cx43表达增加,强调了SDF-1α@PUE水凝胶对巨噬细胞M2型极化的抗炎影响,有助于创造有利的免疫微环境促进心脏修复。进一步评估了SDF-1α@PUE水凝胶在MI大鼠模型中的治疗效果,发现经过28天的治疗后,梗死区域减少,瘢痕百分比降低,心脏重塑减轻,心功能显著改善。

图7.SDF-1α@PUE水凝胶对心肌梗死大鼠模型的治疗效果
2.8 心梗后的长期预后有明显改善
研究发现SDF-1α@PUE具有减小梗死面积、保持心肌收缩性和增加可存活心肌细胞的潜力,同时没有引起血常规、血清炎症因子和病理异常的显著变化,这些表明SDF-1α@PUE在试验中具有长期的生物安全性。在5个月的记录中,与对照组相比,SDF-1α@PUE治疗组显示出较低死亡率。通过心脏病理切片分析和离体灌流心脏系统的评估,证实了SDF-1α@PUE水凝胶对心脏治疗的潜在疗效和延长治疗效益的潜力。研究结果还显示SDF-1α@PUE治疗有助于减小心肌瘢痕形成,防止心脏重塑,提高左室功能,从而改善了心脏功能。

图8.SDF-1α@PUE水凝胶的长期治疗效果
原文链接:
https://doi.org/10.1002/adma.202302686
征文通知: